组织透明化技术使生物学家无需将样本切成薄的连续切片,就能获取高分辨率的三维图像。不过部分技术存在一个主要局限:难以保留内源性荧光蛋白(FPs)的信号。基于溶剂的组织透明化方法需要脱水步骤,会去除组织中的水分子,而水分子是维持荧光蛋白信号所必需的。尽管最近的3DISCO和iDISCO等基于溶剂的技术试图解决这一问题,但这些方法仍只能维持几天的荧光蛋白发光。
其他知名技术如CUBIC、Scale和PACT虽能保留荧光蛋白发光,但需要大量时间投入,且仅适用于小样本组织。SWITCH技术使用强固定剂和高温,会导致荧光蛋白信号丢失。从原理上看,CLARITY方法与荧光蛋白成像的兼容性最佳,但需要自行搭建电泳槽并配备临时冷却系统以防止过热,这对大多数人来说颇具挑战。

X-CLARITYTM组织透明化系统及试剂基于CLARITY原理开发,已经开发出了标准化、简单化并加速组织透明化的每个步骤。X-CLARITYTM组织透明化系统的其中一个组件是电泳组织透明化(ETC)腔室,它配备铂金平板电极和内置冷却系统,可实现高效的组织透明化。使用该系统,一整只小鼠的大脑仅需6小时即可完成透明化处理,同时还能保留内源性荧光蛋白(FP)信号。在本报告中,我们介绍了使用X-CLARITYTM组织透明化系统及试剂进行样本处理以用于三维成像的方案,重点聚焦于荧光蛋白信号的保留。
所有动物实验流程均遵循KBRI IACUC指南开展。选取20周龄的成年Thy1-YFP小鼠,以250mg/kg Avertin(阿佛丁,Sigma公司)对其实施麻醉,随后经心脏依次灌注30mL PBS,再灌注20mL新鲜4%多聚甲醛(流速为10mL/min)。取出大脑组织后,将其置于4℃的4%多聚甲醛中孵育24小时,之后用PBS洗涤并保存于4℃环境中24小时。
技术提示:
后固定是X-CLARITYTM实验protocol中的重要步骤。完整小鼠脑组织需进行至少24小时后固定。过度固定会延长透明化耗时。
后固定的组织需洗涤至少24小时,因为残留的多聚甲醛会在水凝胶聚合过程中与丙烯酰胺发生反应,进而延长透明化耗时。

使用X-CLARITY™水凝胶溶液试剂盒(Logos Biosystems,C1310X)配制水凝胶溶液。将脑组织置于水凝胶溶液中(每个脑组织5mL),在4℃条件下孵育24小时。随后将盛有脑组织的溶液放入X-CLARITY™聚合系统(Logos Biosystems,C20001)中,在37℃、-90kPa的条件下孵育2小时以启动聚合反应。
技术提示:
原始CLARITY与X-CLARITY™组分的核心差异在于水凝胶溶液中是否使用双丙烯酰胺和多聚甲醛(PFA)。双丙烯酰胺与PFA的使用会提升交联密度,但同时也会增加组织透明化耗时。
由于X-CLARITY™组分中没有使用双丙烯酰胺,水凝胶聚合后不会出现凝胶化现象。若原本的液态水凝胶溶液变为黏稠的胶状,即说明丙烯酰胺聚合反应已成功完成。
将包埋在水凝胶中的脑组织用电泳组织透明化溶液(Logos Biosystems,C13001)冲洗,随后将其置于X-CLARITY™组织透明化系统(Logos Biosystems,C10001)的ETC腔室中。让电泳组织透明化溶液在腔室内循环,同时在35℃条件下向小鼠脑组织施加0.7A电流,持续6-12小时。透明化完成后,将脑组织在室温下用PBS溶液过夜冲洗,以去除残留的SDS。
技术提示:
内源性荧光蛋白(FP)信号在高温环境下会降解。为避免过度的焦耳热,需优化电泳过程中施加的电流。使用较低电流以最大程度减少温度升高,不过这可能会影响透明化耗时。
将透明化处理后的脑组织切成1毫米厚的切片或半脑组织来进行免疫染色。将脑组织样本置于抗胶原蛋白IV抗体(1:100,Abcam)的溶液中,在0.1M PBS(含6% BSA、0.2% Triton X-100、0.01%叠氮化钠)中,37℃轻柔摇晃孵育24小时。孵育24小时后,用PBST溶液(1×PBS含0.2% Triton X-100、0.01%叠氮化钠)在37℃下孵育过夜。随后,将样本置于山羊抗兔Cy3 Fab片段(1:250,Jackson ImmunoResearch)和TO-PRO-3(1:1000,ThermoFisher Scientific)碘化物的溶液中,在0.1M PBS(含6% BSA、0.2% Triton X-100、0.01%叠氮化钠)中,37℃轻柔摇晃孵育24小时。最后,在37℃下用PBST溶液过夜清洗。
将染色后的样本用蒸馏水冲洗5分钟,随后将其浸入X-CLARITY™固定剂(Logos Biosystems,C13101)中,在室温下轻柔摇晃孵育1小时。更换固定剂后,样本继续孵育1-2小时。
共聚焦成像,将脑切片放置在35毫米玻璃底培养皿(SPL Life Sciences)中,加入新鲜固定剂,使用LSM 710(Carl Zeiss)共聚焦显微镜,搭配EC Plan-Neofluar 10x/0.3物镜进行成像。使用蔡司ZEN软件处理图像。光片成像,将半脑组织放置在成像腔中,加入新鲜封片溶液,使用Lightsheet Z.1(Carl Zeiss)光片显微镜,搭配EC Plan-Neofluar 5x/0.16物镜进行成像。
ZEN软件用于处理共聚焦成像的图像,Amira 3D 软件(FEI)用于处理光片成像的图像,并将图像渲染成3D视频。
技术提示:
折射率匹配完成后应立即进行荧光成像,以最大程度减少荧光信号损失。染色样本可在固定剂中保存将近3天,而不会出现明显信号衰减;若需更长时间的保存,需将样本置于PBS溶液中4℃保存。
经过X-CLARITY™系统和试剂进行组织透明化处理,内源性Thy1-YFP蛋白稳定且保存完好。抗胶原蛋白IV抗体和TO-PRO-3碘化物可有效渗透样本。
光片成像结果被渲染为高分辨率3D视频,可通过以下链接查看:A journey through a Thy1-YFP mouse brain.
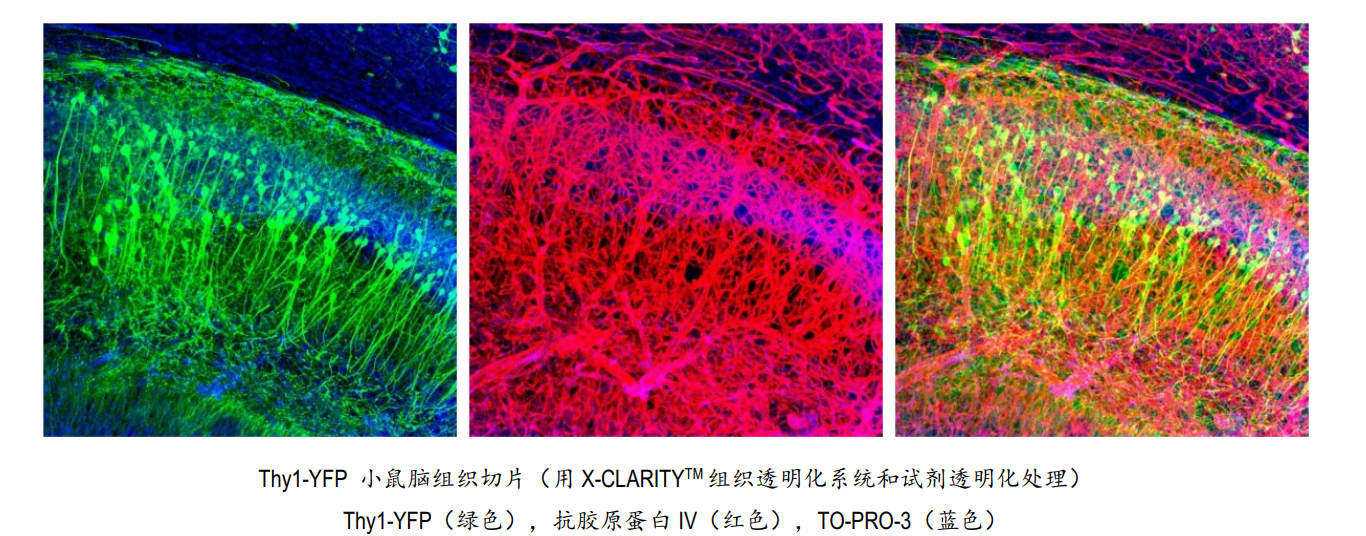
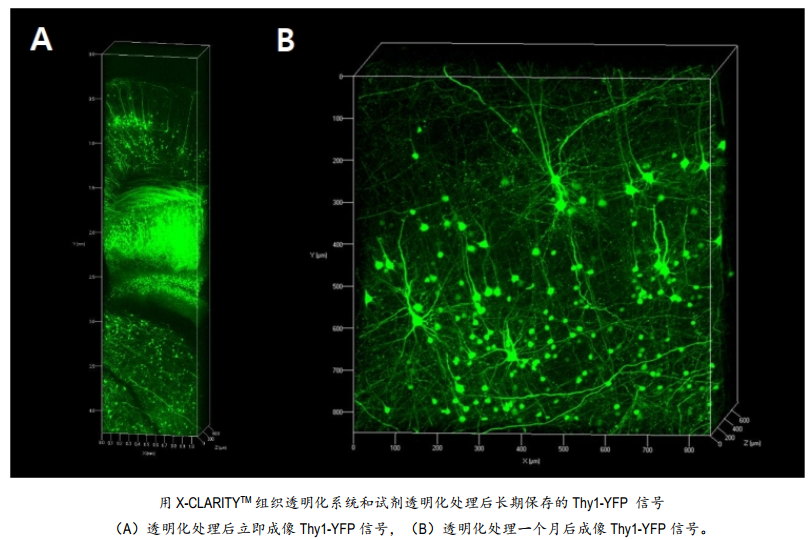
本文描述的是一套从透明化小鼠大脑中获取内源性荧光蛋白信号的逐步实验方案。如文所示,使用X-CLARITYTM组织透明化系统和试剂处理后,Thy1-YFP信号得以良好保留,且样本透明化处理一个月后,信号仍保持稳定。X-CLARITYTM组织透明化系统配备带有铂金平板电极的ETC腔室,可产生密集且稳定的电流,实现极快的透明化速度和一致的透明化效果。结合集成冷却系统,该系统能有效保留内源性荧光蛋白的荧光信号,可使大样本的三维容积成像的分辨率高达单细胞水平,从而提升数据质量。

1. Lee,E.et al. ACT-PRESTO: Rapid and consistent tissue clearing and labeling method for 3 dimensional (3D) imaging. Scientific Reports 6,18631 (2016).
2. [Application Note] An automated and high-throughput polymerization solution for downstream tissue clearing: the X-CLARITY Polymerization System,Logos Biosystems (2016).
3. Richardson,D.& Lichtman,J. 2015. Clarifying tissue clearing. Cell162,246-257 (2015).
4. Jun,Li et al. Fast immune-labeling by electrophoretically driven infiltration for intact tissue imaging.
5. Chung,K. & Deisseroth,K. CLARITY for mapping the nervous system. Nature Methods 10, 508-513 (2013).
声明:上述材料是参照英文版应用技术文档,利用百度文心助手工具,结合最新产品信息整理而成。如有翻译不准确或者不当之处,敬请批评指正。英文版应用技术文档请登录www.logosbio.com或者查询。
AppNote-Preserving-endogenous-fluorescen
利用X-CLARITY™系统和试剂进行脑组织透明化来保留内源性荧光蛋白用于三维容